
Цялото съдържание на iLive е медицински прегледано или е проверено, за да се гарантира възможно най-голяма точност.
Имаме строги насоки за снабдяване и само свързваме реномирани медийни сайтове, академични изследователски институции и, когато е възможно, медицински проучвания, които се разглеждат от специалисти. Имайте предвид, че номерата в скоби ([1], [2] и т.н.) са линкове към тези проучвания.
Ако смятате, че някое от съдържанието ни е неточно, остаряло или под съмнение, моля, изберете го и натиснете Ctrl + Enter.
Производни на талидомид водят до смърт на резистентни ракови клетки
Последно прегледани: 02.07.2025
 ">
">Проучване, проведено от Университета „Гьоте“ във Франкфурт, сочи към възможността производните на талидомид потенциално да се използват за лечение на рак. Талидомид се е продавал като хапче за сън през 50-те години на миналия век. По-късно става известен с това, че причинява тежки вродени дефекти в ранните етапи на бременността.
Молекулата е известна също с това, че маркира протеини в клетката за унищожаване. Като част от настоящото изследване, учените създадоха производни на талидомид. Те успяха да покажат, че тези вещества влияят върху разрушаването на протеини, отговорни за оцеляването на раковите клетки.
Може би никоя друга молекула не е имала толкова бурно минало като талидомид. Той е бил основната съставка в лекарство, одобрено в много страни през 50-те години на миналия век като успокоително и сънотворно. Но скоро станало ясно, че бременните жени, приемащи талидомид, често раждат бебета със сериозни деформации.
Въпреки това, през последните десетилетия медицината отново възлага големи надежди на него. Проучванията показват, наред с други неща, че той инхибира растежа на кръвоносните съдове и следователно е потенциално подходящ за отрязване на туморите от хранителната им среда. След това се оказа много ефективен и при лечението на множествен миелом, злокачествени тумори в костния мозък.
„Сега знаем, че талидомидът може да се нарече „молекулярно лепило““, обяснява д-р Синлай Ченг от Института по фармацевтична химия към Университета Гьоте във Франкфурт. „Това означава, че той е способен да хване два протеина и да ги съедини.“
Това е особено интересно, защото един от тези протеини е един вид „машина за етикетиране“: той прикрепя недвусмислен етикет „БОКЛУК“ към друг протеин.
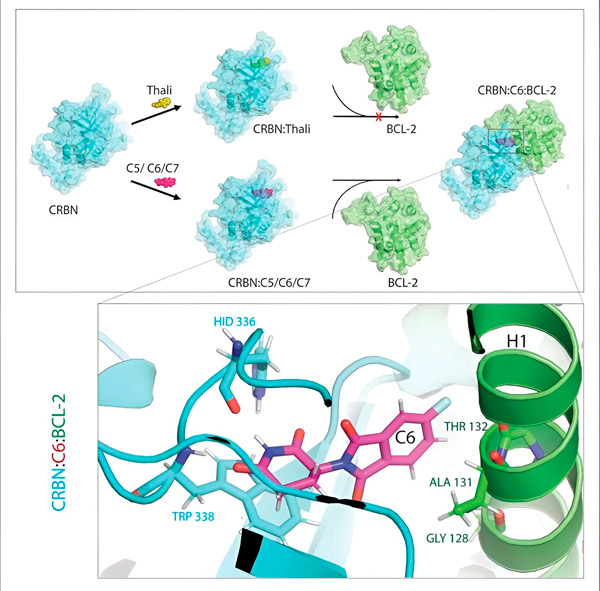
Производните на талидомид C5, C6 и C7 променят CRBN, „машината за маркиране“, така че той да може да се свърже с BCL-2. По този начин молекулата BCL-2 е маркирана за разграждане – възможна нова стратегия за борба с рака. Автор: Д-р Синлай Ченг.
Системата за изхвърляне на отпадъци в клетката разпознава този маркер: Тя хваща маркираната протеинова молекула и я раздробява. „Този механизъм обяснява различните ефекти на талидомид“, казва Ченг. „В зависимост от това кой протеин е маркиран, той може да причини деформации по време на ембрионалното развитие или да унищожи злокачествени клетки.“
Този механизъм открива големи възможности за медицината, тъй като раковите клетки зависят от определени протеини, за да оцелеят. Ако те могат да бъдат систематично насочени и раздробени, може би болестта би могла да бъде излекувана. Проблемът е, че молекулярното лепило е доста специфично.
Един от свързващите му партньори винаги е маркиращата машина на клетката или, на научен език, E3 лигаза, наречена CRBN. Само много малко от многото хиляди протеини в тялото могат да бъдат вторият партньор – кои от тях, зависи от лепилото.
„И така, създадохме серия от производни на талидомид“, казва Ченг. „След това тествахме дали имат адхезивни свойства и ако е така, срещу кои протеини са ефективни.“ За да направят това, изследователите добавиха своите производни към всички протеини в култивираната клетъчна линия. След това те наблюдаваха кои от тези протеини се разграждат в присъствието на CRBN.
„В процеса идентифицирахме три производни, които биха могли да маркират клетъчен протеин, много важен за разграждането, BCL-2“, обяснява Ченг. „BCL-2 предотвратява активирането на програмата за самоунищожение на клетките, така че ако не е там, клетките умират.“
Ето защо BCL-2 отдавна е във фокуса на изследванията на рака. Има дори лекарство за левкемия, наречено венетоклакс, което намалява ефективността на BCL-2 и по този начин кара мутиралите клетки да се самоунищожат.
„Въпреки това, в много ракови клетки самият BCL-2 е мутирал. В резултат на това венетоклаксът вече не инхибира протеина“, казва Ченг. „Успяхме да покажем, че нашите производни също така сигнализират за разграждане на тази мутирала форма. Освен това, нашите партньори от Института за биофизика „Макс Планк“ симулираха взаимодействието на производни на талидомид с BCL-2 на компютър. Това показа, че производните се свързват с напълно различни места от венетоклакса - резултат, който по-късно успяхме да потвърдим експериментално.“
Изследователите също така тестваха своите съединения върху плодови мушици с ракови клетки. Процентът на оцеляване на мухите, третирани по този начин, беше значително по-висок. Ченг обаче предупреждава да не се надяваме прекалено много, тъй като тези резултати все още са фундаментално изследване. „Въпреки че показват, че модифицираните молекули на талидомида имат голям терапевтичен потенциал, все още не можем да кажем дали те ще се докажат на практика в даден момент.“
Резултатите от изследването са публикувани в списанието Cell Reports Physical Science.
