
Цялото съдържание на iLive е медицински прегледано или е проверено, за да се гарантира възможно най-голяма точност.
Имаме строги насоки за снабдяване и само свързваме реномирани медийни сайтове, академични изследователски институции и, когато е възможно, медицински проучвания, които се разглеждат от специалисти. Имайте предвид, че номерата в скоби ([1], [2] и т.н.) са линкове към тези проучвания.
Ако смятате, че някое от съдържанието ни е неточно, остаряло или под съмнение, моля, изберете го и натиснете Ctrl + Enter.
Как ембрионът „захапва“ майчината тъкан: механиката на имплантацията при хора, заснета в реално време за първи път
Последно прегледани: 23.08.2025
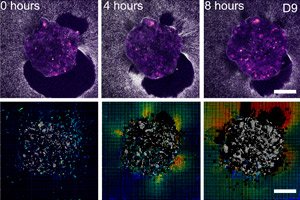 ">
">Учени от Барселона (IBEC, Dexeus Mujer) и Тел Авив показаха за първи път в реално време и в 3D как човешки ембрион се прикрепя към „маточното скеле“ и буквално дърпа и преструктурира околната тъкан. За да направят това, те създадоха деформируема ex vivo платформа (колагенови/ECM гелове) и приложиха микроскопия с тракционна сила директно върху живи човешки и миши ембриони. Ключовото откритие: моделът на силите е видово специфичен, а самите ембриони са механочувствителни: те реагират на външни механични сигнали чрез преструктуриране на цитоскелета и промяна на ориентацията на растеж.
Предистория на изследването
Имплантацията е „пречката“ в човешката репродукция: именно на този етап както естествените зачевания, така и опитите за ин витро оплождане най-често се провалят. В същото време, човешката имплантация е интерстициална: ембрионът не просто се „залепва“, а е напълно вграден в ендометриума - биохимично и механично сложен процес, но доскоро почти ненаблюдаван в живите системи при хората. Следователно, механиката на адхезията и инвазията оставаше „черна кутия“ и заключенията често се правеха въз основа на косвени маркери или данни от животински модели.
Класическата имплантационна биология е разчитала до голяма степен на мишката, но съществуват фундаментални разлики между видовете, от ориентацията на бластоцистата до дълбочината на имплантация и модела на клетъчните сили. При мишките имплантацията е по-„повърхностна“, с преференциални посоки на изместване на тъканите; при хората тя е отчетливо инвазивна, с многофокални сили на сцепление около ембриона. Тези разлики показват, че мишият модел не винаги е мащабируем за хора, особено що се отнася до механиката. Необходими са били директни наблюдения на човешкия ембрион в деформируема среда.
Технологичният пробив е осъществен чрез комбиниране на деформируеми 2D/3D матрици (колаген/ECM) и микроскопия с тракционна сила с дългосрочно високочестотно изобразяване. Тази „изкуствена матка“ прави възможно буквалното виждане и измерване на това как ембрионът дърпа, преструктурира и „пробива“ околната тъкан – и как реагира на външни механични сигнали (механочувствителност). Това отваря пътя към нови критерии за оценка на имплантационния потенциал и за фина настройка на условията на ембриотрансфер.
Приложен е контекстът: ако механичните свойства на средата и моделът на ембрионалните сили са свързани с успеха на имплантацията, тогава при ин витро оплождането е възможно целенасочено да се избере твърдостта/съставът на матрицата, да се вземат предвид времевите прозорци на трансфера и дори да се използват показатели за „сила“ като допълнителен маркер за селекция. Успоредно с това, подобни платформи ще помогнат да се обясни делът на ранните загуби на бременност, когато биохимията е „нормална“, но механиката на адхезията не е. Всичко това прави директните 3D наблюдения на човешката имплантация не просто красиво видео, а нов инструмент за репродуктивната медицина.
Защо това е важно?
Неуспешната имплантация е една от основните причини за безплодие и до 60% от спонтанните аборти. Въпреки биохимичния напредък в ин витро оплождането, механиката на този процес при хората остава „черна кутия“. Нов подход ни позволява да видим силите и траекториите на имплантацията на ембрионите и осигурява основа за подобряване на условията за подбор и трансфер на ембриони.
Как беше направено
Изследователите сглобили „изкуствена утроба“ - мека, прозрачна и деформируема среда, в която тъканоподобна матрица видимо се измества под въздействието на ембрионални сили. След това последвала непрекъсната микроскопия и компютърен анализ на изместванията на влакната.
- 2D и 3D платформи: в 3D ембрионът се вгражда незабавно в матрицата (етапът на прикрепване се „прескача“), което позволява да се види пробиването в дебелината на тъканта.
- Висока „оцеляване и проникване“ в 3D: около 80% успешно нахлуване (ограничено от близостта до стъкло).
- Картите на тракцията и дигиталната корелация на обема показват амплитудите и посоките на изместванията около ембриона - по същество „отпечатък“ на силата във времето.
Какво точно беше открито (накратко и точка по точка)
1) Видоспецифична механика на имплантация
- Човек: ембрионът се вмъква в матрицата, създавайки множество огнища на сцепление и формирайки радиално равномерни измествания около себе си; дълбочината на инвазия е до 200 µm.
- Мишка: ембрионът се разпространява главно по повърхността с ясно изразени главни посоки на изместване.
2) Ембрионът усеща механиката на околната среда
- Външни сили → отговор: в човешкия ембрион - набиране на миозин и насочени клетъчни псевдоподии; в мишката - въртене на оста на имплантация/растеж към източника на външна сила (ориентация на оста PD).
- Механочувствителни маркери: при мишки, промени в локализацията на YAP в трофобласта; заедно това показва механочувствителна верига за обратна връзка.
3) Връзката между силата и успеха на имплантацията
- По-малко изместване на колагена → по-лош напредък на имплантацията при човешки ембриони.
- Интегрини - "свързващото звено" на силата: Блокадата на RGD пептида/инхибирането на Src при мишки намалява дълбочината/площта на имплантация.
Как изглежда внедряването?
- На 2D и 3D платформи около ембриона се образува нарастващ „ореол“ от измествания на влакната; картата на сцепление пулсира, сякаш ембрионът „сканира“ обкръжението си.
- Върху стъклото човешкият ембрион образува плосък израстък, но в мека матрица той остава по-сферичен и отива по-дълбоко - както в живата тъкан.
Какво дава това на практиката (перспективи за ин витро и не само)
Идеята е проста: имплантацията не е само „химия на рецепторите“, но и механиката на адхезията и сцеплението. Това означава, че можем да оптимизираме:
- Твърдост на материалите и средата по време на тестове за култивиране/имплантационен потенциал;
- Нови маркери за селекция на ембриони - базирани на траектории и амплитуда на измествания в „умната“ матрица;
- Обучение/модулация на матката (напр. чрез нежни механични сигнали) за подобряване на адхезията без агресивни интервенции.
Внимание: работата ex vivo не е „вътре в утробата“. Но самият факт, че външен механичен сигнал променя ориентацията на имплантацията/организацията на осите, отваря пътя към персонализирани условия на ембриотрансфер.
Ограничения
- Моделът ex vivo не отчита имунната, хормоналната и съдовата динамика на реалния ендометриум;
- Матригелът/колагенът определят набор от свойства (твърдост, вискоеластичност, състав), трудно е да се променят само с един параметър;
- Етичните ограничения за изследвания върху хора (до 14 дни) ограничават дългосрочното наблюдение. Въпреки това, високото съответствие с известните in vivo начини на имплантация (интерстициална при хора срещу повърхностна при мишки) повишава доверието в модела.
Заключение
Човешкият ембрион активно „дърпа“ и „пробива“ пътя си в майчината тъкан, а механичните сигнали от околната среда могат да преконфигурират поведението му. Моделът на силите и стратегията на имплантация са различни при хората и мишките - и това може да обясни защо мишият модел не винаги предсказва успешна имплантация при хората. Механиката вече е пълноправен играч в ранната ембриология и репродуктивната медицина.
Източник: Godeau AL et al. Силата на сцепление и механочувствителността медиират видово-специфични модели на имплантация в човешки и миши ембриони. Science Advances 11(33): eadr5199 (15 август 2025 г.). DOI: 10.1126/sciadv.adr519
