
Цялото съдържание на iLive е медицински прегледано или е проверено, за да се гарантира възможно най-голяма точност.
Имаме строги насоки за снабдяване и само свързваме реномирани медийни сайтове, академични изследователски институции и, когато е възможно, медицински проучвания, които се разглеждат от специалисти. Имайте предвид, че номерата в скоби ([1], [2] и т.н.) са линкове към тези проучвания.
Ако смятате, че някое от съдържанието ни е неточно, остаряло или под съмнение, моля, изберете го и натиснете Ctrl + Enter.
Изкуственият интелект открива рак на простатата в ранен стадий, пропуснат от патолози
Последно прегледани: 23.08.2025
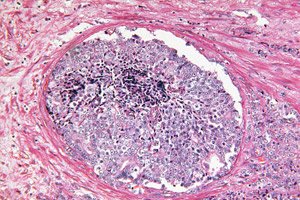 ">
">Научни доклади показват, че изкуственият интелект може да разпознава скрити морфологични следи от тумор в биопсии на простатата, които преди това са били считани за доброкачествени от патолог. Модел на дълбоко обучение, обучен с помощта на слабо контролиран подход, прогнозира кои мъже с повишен PSA ще развият клинично значим рак на простатата (ISUP > 1) през следващите 30 месеца и кои ще останат без рак поне 8 години. Това отваря вратата за ранна стратификация на риска веднага след първоначална „чиста“ биопсия и може да помогне да се реши кой наистина се нуждае от повторни инвазивни процедури и засилено наблюдение.
Предистория на изследването
Първичната иглена биопсия на простатата често дава фалшиво отрицателни резултати: значителна част от клинично значимия рак остава „извън екрана“, особено при традиционната системна TRUS биопсия. Въвеждането на ЯМР насочване е увеличило дела на откриване на клинично значим рак и е намалило броя на ненужните повторни процедури, но дори и при съвременни стратегии, някои агресивни тумори остават неоткрити. Клиничната дилема остава същата: кой трябва да бъде наблюдаван след „чиста“ биопсия и кой трябва да бъде насочен за ранна повторна биопсия, за да не се забави диагнозата и да не се претоварят пациентите с инвазивни интервенции.
Биологичната основа за решаването на този проблем е феноменът TINT (тумор-инструктирана/показваща нормална тъкан): туморът „преконфигурира“ околните привидно нормални тъкани на органа, оставяйки в тях слаби, но систематични следи - от стромално ремоделиране и хипоксия до метаболитни промени. Тези промени са описани в експериментални модели и при пациенти с рак на простатата и корелират с агресивността на тумора, което прави „нормалната“ тъкан потенциален източник на диагностични сигнали, дори ако в биопсичната проба няма очевидни ракови жлези.
Методите за дигитална патология и дълбоко обучение са насочени към извличане на такива „фини“ полеви характеристики от стандартни H&E срези. За разлика от класическата морфология, която се фокусира върху очевидни туморни структури, алгоритмите могат да уловят разпределени модели в стромата и епитела, свързани с наличието на тумор в друга част на органа. Това отваря пътя за стратификация на риска веднага след отрицателна биопсия: високият „скор“ по скалата на Glass предполага целесъобразност на ранна повторна биопсия или насочване с ЯМР, а ниският подкрепя по-щадящо наблюдение.
Това е идеята зад ново проучване в Scientific Reports: авторите тестват дали изкуственият интелект може да предскаже клинично значим рак на простатата през следващите 30 месеца въз основа на морфологични сигнали от TINT биопсии. Работата надгражда линията на вече представен препринт и формира приложна основа за внедряването на „полеви“ цифрови биомаркери при насочване на пациентите след първоначална „чиста“ биопсия.
Как беше направено: дизайн, данни, алгоритъм
Авторите ретроспективно събраха кохорта от 232 мъже с повишен PSA и първоначално заключение „доброкачествен“ при иглена биопсия (след технически контрол, 213 пациенти и 587 среза бяха включени в окончателния анализ; биопсии 1997-2016, Умео, Швеция). Всеки пациент беше съпоставен с „огледална“ двойка по възраст, година на поставяне на диагнозата и ниво на PSA: половината бяха диагностицирани с рак на простатата по-късно (≤30 месеца), другата половина останаха без рак поне 8 години. H&E слайдовете бяха дигитализирани (20×), нарязани на 256×256 пикселни плочки и подадени към CLAM (Clustering-constrained Attention Multiple-Instance Learning) - съвременна слабо контролирана схема, където е известна само съдбата на пациента, а не маркировката на всеки пиксел. Характеристиките бяха извлечени от ResNet18, предварително обучен върху 57 хистопатологични набора от данни. Крайната точка е двоична: нисък риск (доброкачествен/ISUP1) срещу висок риск (ISUP2-5).
Точност на прогнозирането
В независим тест моделът постигна AUC от 0,81 за всички препарати и AUC от 0,82 на ниво пациент. При праг, който осигуряваше приемлив баланс, чувствителността беше 0,92 с процент на фалшиво положителни резултати от 0,32 (на ниво пациент). С други думи, сред хората, чиято първоначална биопсия „не е била успешна“, изкуственият интелект правилно маркира по-голямата част от тези, за които скоро беше потвърдено, че имат клинично значим рак, макар и с цената на някои фалшиви аларми. За клиниката това е сигнал: „доброкачествен“ отговор на биопсия ≠ нулев риск и той може да бъде количествено стратифициран чрез дигитално стъкло.
Какво точно „забелязва“ изкуственият интелект в „нормалната“ тъкан?
Интерпретацията чрез UMAP и карти на вниманието показа, че промените в стромата са най-информативни:
- Повече колаген в стромата (уплътняване на матрикса, „фиброза“);
- По-малко гладкомускулни клетки около жлезите;
- По-рядко срещани са фините сигнали в жлезистия епител, вероятно под наличната резолюция за намаляване на семплирането.
Този модел се вписва в концепцията за TINT (тумор-инструктирана/показваща нормална тъкан): дори „нормата“ в орган, където е скрит тумор, се преконфигурира под негово влияние и се различава от „нормата“ в орган без тумор. Ракът е не само огнище, но и поле, а изкуственият интелект се научава да разчита ефекта на полето.
Как подходът е полезен на практика - потенциални сценарии
- Повторна биопсия, базирана на риска: висок процент на изкуствен интелект върху „чисто“ стъкло - аргумент в полза на ранна повторна биопсия или насочване с ЯМР вместо изчакване.
- Персонализиране на мониторинга: Ниската скорост балансира тревожността след „граничен“ ЯМР и позволява модериране на интензивността на мониторинга.
- Обучение по TINT модел: Картите на вниманието и интерактивните наслагвания помагат на патолозите да виждат фините полета около рака, подобрявайки последователността на докладите.
Важно е да се разберат ограниченията
Това е един център в Северна Швеция (предимно бяло население), дизайнът е ретроспективен, изходните биопсии са извършени без ЯМР насоки (систематични TRUS биопсии), а маркерите са бъдещи резултати, а не „скрит тумор на едно и също стъкло“. Все още няма външна валидация в независими центрове/скенери, нито пък има проспективно проучване на ефекта на алгоритъма върху клиничните решения и резултати. Процентът на фалшиво положителни резултати остава значителен - моделът не замества лекаря, а добавя вероятностен слой за споделено вземане на решения.
Какво следва: Пътна карта за внедряване
- Многоцентрова външна валидация (различни скенери, протоколи, етнически групи).
- Проучвания за перспективни решения: променя ли оценката по AI траекторията на пациента (време до поставяне на диагноза, брой ненужни повторни биопсии, свръх/недостатъчна диагноза).
- Интеграция с ЯМР и клиника: комбинирани модели (PSA, ЯМР PIRADS, клинични фактори + TINT оценка според H&E).
- Технически стъпки: стандартизация на дигитализацията, контрол на отклонението на данните, обяснимост (наслагване на вниманието върху рутината).
Източник: Chelebian E., Avenel C., Järemo H., Andersson P., Bergh A., Wählby C. и др. Откриване на тумор, показващ морфологични промени в доброкачествени биопсии на простатата чрез изкуствен интелект. Научни доклади (Nature Portfolio), публикувани на 21 август 2025 г. DOI: https://doi.org/10.1038/s41598-025-15105-6
